来自上海的研究团队通过研究1月下旬至2月期间的新冠患者的病毒样本,发现新冠病毒可划分为两大分支,分别从一个共同祖先独立进化而来。不过,这两大分支病毒在临床上对患者致病效应无显著区别。COVID-19疾病发展严重程度的决定因素主要还是与患者年龄、基础疾病、淋巴细胞减少和相关的细胞因子风暴等密切相关。
上述研究来自当地时间5月20日顶级学术期刊《自然》(Nature)以“加快评审文章 (Accelerated Article Preview) ”形式在线发表的一项研究,题为“Viral and host factors related to the clinic outcome of COVID-19”。该研究由来自复旦大学附属上海市公共卫生临床中心、上海交通大学附属瑞金医院、上海血液学研究所、医学基因组学国家重点实验室、中科院植物生理生态研究所、上海巴斯德研究所和上海营养与健康研究所等多家上海科研和医疗单位合作完成。研究团队分析了1月下旬至2月期间,在上海公共卫生临床中心收治的326例新冠患者的SARS-CoV-2病毒样本。
通讯作者为上海公共卫生临床中心党委书记卢洪洲教授,中国工程院院士、上海交通大学医学院教授、上海血液学研究所所长陈赛娟,与上海交通大学王升跃研究员。
研究团队对上海公共卫生临床中心于1月20日至2月25日期间收治的326例新冠肺炎确诊病例的临床、分子和免疫学资料进行了分析。自1月27日收到第一批样本起,瑞金医院的转化医学国家重大科技基础设施重大疾病基因组研究平台在一个多月时间内完成了112个病例的SARS-CoV-2基因组高质量测序。这些序列与全球流感数据共享计划(GISAID)中的基因组序列类似,呈现较为稳定地进化过程,显示该病毒可能在疫情早期就已适应在人类宿主中传播。
研究同时发现,疫情早期阶段存在两种有不同接触史的主要病毒分支,但两个分支的传播性、致病性和临床表现等方面无显著差异,未发现与COVID-19重症患者有显著相关的病毒变异序列。
从临床和免疫学研究发现,COVID-19患者淋巴细胞明显减少,尤其是重症患者CD4+和CD8+T细胞呈显著进行性下降趋势,且炎性细胞因子IL-6和IL-8明显增高。
研究团队认为,COVID-19疾病发展严重程度的决定因素主要与患者年龄、基础疾病、淋巴细胞减少和相关的细胞因子风暴密切相关,这些因素成为疾病向重症转变的关键预警因子。依据上述临床分析采取早期针对性干预措施,将有助于阻止疾病向重症发展。
新冠病毒稳定进化,可能在疫情早期已适应在人类宿主中传播
研究定义了四类感染病例。5例患者为无明显发热、呼吸系统症状或放射学表现的无症状患者。大部分患者(293例)为轻症患者,有发热和肺炎表现。12例为重症患者,在24-48小时内出现呼吸困难和肺内毛玻璃样阴影扩大的症状。另有16例患者恶化为急性呼吸窘迫综合征(ARDS),需要机械通气或体外膜氧合(ECMO),属于危重患者。
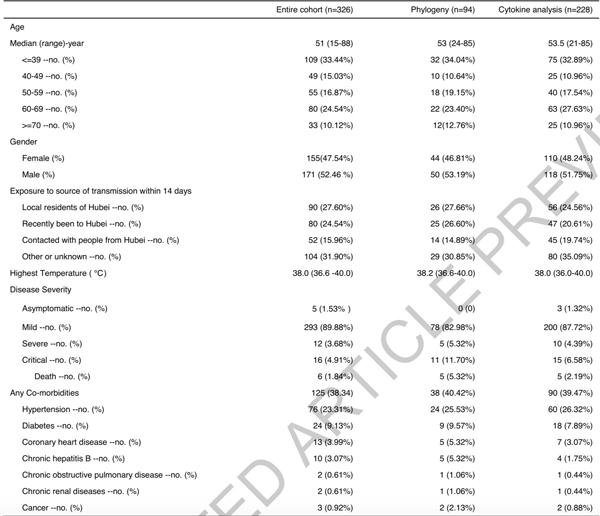
截至4月1日,315名患者(96.63%)已出院,6人(1.84%)死亡。
研究团队对112个样本(痰、口咽拭子)进行测序,与全球第一个公布的基因组(Wuhan-Hu-1)相比,在9个蛋白编码区共鉴定出66个同义变异和103个非同义变异。ORF1ab、S、ORF3a、E、M和ORF7a的替换率相似(约3.5×10^-4每个位点每年),而ORF8(9.51×10^-4每个位点每年)和N(1.05×10^-3每个位点每年)的变异率更高。
在来自上海样本基因组中重复出现的突变的与GISAID数据库中已公布的病毒序列一致,呈现较为稳定的进化过程,显示该病毒可能在疫情早期就已适应在人类宿主中传播。
两大分支新冠病毒,最早疫情发生并不局限于华南海鲜市场
随后,研究团队使用了其中的94例病毒基因组和GISAID数据库中的221个SARS-CoV-2序列进行系统发育分析。研究确定病毒主要为两大分支,两大分支中均包含来自20191年12月初诊断的病例;分支I包括几个亚支,分支II与分支I的区别在于两个相关的变异ORF8:p.84LS (28144TC)和ORF1ab:p.2839S (8782CT)。
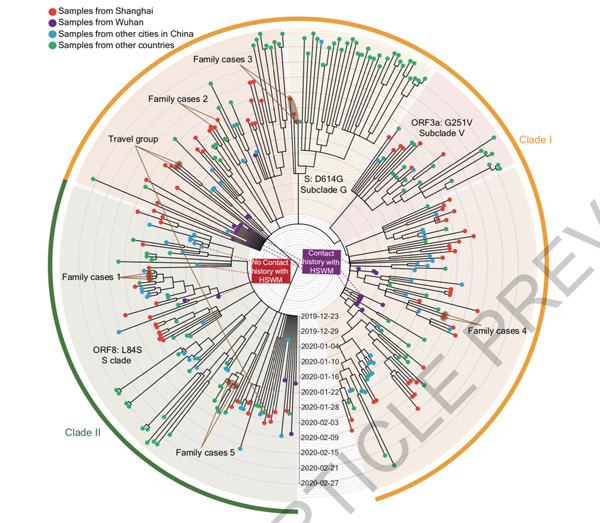
上海样本的序列在两个主要分支及其亚支中均有发现,研究认为这表明上海的新冠病例有多个病毒来源。在上海没有观察到明显的分支/亚支扩张。
此外,确认有华南海鲜市场接触史的6位患者均集中在其中一个分枝中(分支 I),同期诊断的另外3例和华南海鲜市场没有接触史的病例均属于分支II,提示疫情发生并不局限于华南海鲜市场。
论文指出,这两种主要的单倍型可能代表了来自于2019年12月初在武汉由共同祖先独立进化而来的两种谱系,其中只有一种(分支I)和华南海鲜市场接触有关,市场内密集的摊位、摊贩和顾客可能促进了人际传播。
与此一致的是,一项针对12月18日前武汉地区最早的病例流行病学调查发现,2例患者与华南海鲜市场有关联,5例患者与之无关联。他们的系统发育分析表明,疫情最早可能发生在2019年11月下旬。
研究团队还比较了感染分支I或分支II病毒患者的临床表现。他们发现,在疾病严重程度(p=0.88)、淋巴细胞计数(p=0.79)、CD3 T细胞计数(p=0.21)、C反应蛋白(p=0.83)或D-二聚体(p=0.19)以及发病后排毒时间(p=0.79)方面均没有统计学差异。因此,研究团队认为,这两分支病毒尽管基因组序列发生变化,但表现出相似的致病效应。
同样,在疾病严重程度和13个最常见的变异(同义和非同义)之间也没有发现显著的相关性。
与COVID-19疾病发展严重程度相关的宿主因素
这项研究的一个显著特征是,部分感染者(5例,1.53%)虽然可以检测到明显的排毒,但未出现明显症状。相比之下,在轻度和危重症病例中观察到肺部单侧和双侧混浊病变,危重症患者仅在两天内就迅速恶化。
研究团队进一步分析了患者的免疫生化指标。COVID-19的一个显著特征是进行性淋巴细胞减少,尤其是重症和危重症(入院后初步检测结果,p=6×10^-6)。对淋巴细胞亚型的详细分析显示,CD3+ T细胞受影响最显著(p10^-6), CD4+和CD8+ T细胞具有相似的趋势(CD4+ T细胞,p10-6;CD8+ T细胞,p=1×10^-5)。
值得注意的是,T淋巴细胞的变化不仅在危重病例中有统计学意义,而且在其他三类(无症状、轻度和重度)中也有统计学意义(CD3+ T细胞,p=0.013;CD8+ T细胞,p=0.004)。相比之下,CD19+ B细胞虽然在危重患者中有显著下降(p=1×10^-5),但在无症状、轻症、重症病例中无明显变化(p=0.47)。
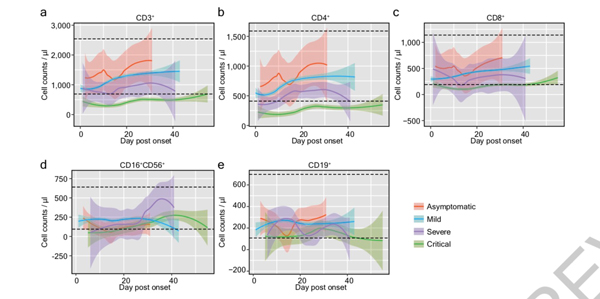
研究团队进一步检查了每组数据后得出,随着病情的恶化,CD3+ T淋巴细胞(在发病后第7、8、11、14-18、22-25、28、29天检测)呈逐渐下降趋势(p0.05),CD4+和CD8+ T细胞也呈类似趋势。然而,NK细胞(CD16+、CD56+)或B细胞(CD19+)没有这种现象。
接下来,研究比较了共病组的临床参数,发现虽然共病组的中位年龄较高(p=0.02),但共病组疾病进一步发展的风险的确显著提高(p=0.01)。事实上,单变量逻辑回归分析表明年龄(p 0.0001)、入院时淋巴细胞计数(p 0.0001),合并症(p = 0.01)和性别(p = 0.014)都是与新冠严重程度相关的主要因素。多变量分析则表明,年龄(p = 0.002)和淋巴细胞减少(p = 0.002)是两个主要的独立因素,而合并症没有达到统计学意义。
研究团队在入院和治疗期间检测了患者血清中11个细胞因子(IFN-α、IFN-γ、IL-1β、IL-2、IL-4、IL-5、IL-6、IL-8、IL-10、IL-12和IL-17)的水平。其中,IL-6(p10^-6)和IL-8(p=1×10^-5)变化最为显著。值得注意的是,这两种细胞因子与淋巴细胞计数呈负相关关系。
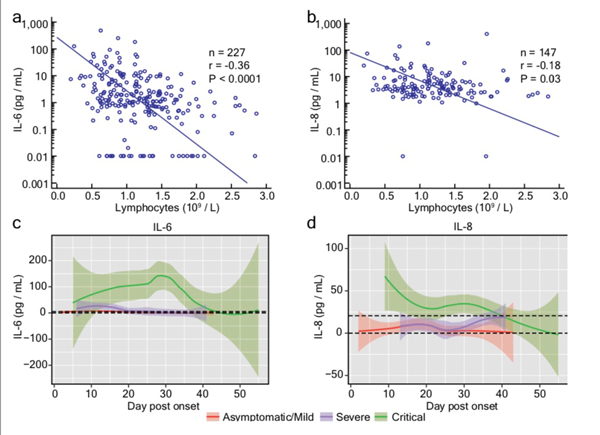
此外,研究团队结合各组细胞因子的纵向数据,绘制其随发病后时间的波动模式。他们收集了每位患者发病后第6天至第10天的最高IL-6数据,并将危重患者与非危重患者进行了比较。危重症患者组IL-6水平显著升高(p=0.001)。从发病后第16天至第20天,患者IL-8水平也有类似的显著差异(p=0.006)。
研究认为,这些数据表明,炎症细胞因子和SARS-CoV-2感染的发病机制之间有很强的联系。
研究在讨论环节指出,这项研究进一步证实发现,CD3+ T细胞是感染患者的主要受抑制细胞类型,而CD19+ B细胞和CD16+CD56+NK细胞受抑制较少。事实上,淋巴细胞减少,尤其是CD4/CD8细胞数量减少,也是SARS-CoV-2感染的主要表现。
此外,研究对主要细胞因子的纵向监测表明,IL-6和IL-8与淋巴细胞计数呈负相关,IL-6动力学与疾病严重程度高度相关。
当然,目前病毒活性、细胞因子释放与淋巴细胞减少的关系尚不清楚。研究团队假设,包括“细胞因子风暴”和CD3+ T淋巴细胞减少在内的针对SARS-CoV-2的免疫病理反应,可能至少在一定程度上构成了疾病进展和死亡的潜在机制。
 简体中文
简体中文






